近日,深圳理工大学(筹)药学院副教授、中国科学院深圳先进技术研究院医药所研究员殷勤团队联合香港中文大学(深圳)成贵娟教授团队首次实现了对光诱导Pd催化丁二烯双官能化过程中亲核和亲电试剂两部分的不对称控制。相关成果于4月20日在线发表于化学领域权威期刊Angew. Chem. Int. Ed.(点击文末“阅读原文”阅读论文)。
研究发现光诱导Pd催化丁二烯与吲哚的串联不对称去芳构化反应能高效构筑结构新颖的手性吲哚啉化合物库,后续的药物活性测试也证实部分合成的化合物针对多类肿瘤细胞具有微摩尔级别的活性(活性测试部分工作还未公开发表)。
该研究进一步扩展了手性氮杂环化学空间为药物研发提供了潜在的新物质基础。
到目前为止,光学纯螺环吲哚啉化合物主要依赖在过渡金属与手性配体的共同催化下,通过分子内环化反应构建。然而,由于分子内的反应需要复杂的反应和底物设计,因此往往需要繁琐的底物制备。
近年来,光催化作为一种绿色高效的合成方法被广泛研究和应用,特别是在光诱导Pd催化的不对称合成领域得到显著发展。目前,传统的依赖于双电子氧化还原化的钯催化已成为选择性构建碳-碳键和碳-杂键最广泛和最有用的方法之一。
相比之下激发态钯催化最近作为一种替代策略出现可以实现与基态钯催化互补的新型转化。
在Gevorgyan、Glorius、南开大学资伟伟等课题组前期关于光诱导钯催化丁二烯转化工作的启发下,并基于前期对于手性氮杂环精准合成的相关课题,殷勤团队设计了吲哚衍生的芳基溴与丁二烯及其衍生物的分子间串联环化反应,发现蓝光激发和手性钯络合物的催化能够顺利得到含有连续手性中心的螺环化合物。反应具有较广的底物普适性以及优秀的不对称控制。
该研究首次实现了光诱导Pd催化的芳基溴和丁二烯反应,突破了以往工作使用烷基卤代物的限制。研究还首次实现了对光诱导Pd催化下丁二烯双官能化过程中亲核和亲电试剂两部分的不对称控制,取得优秀的非对映选择性和对映选择性控制。
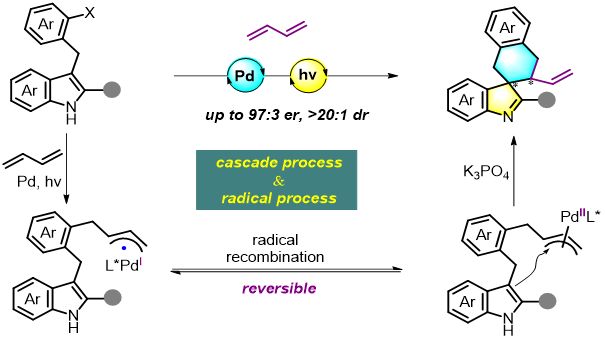
研究内容示意图
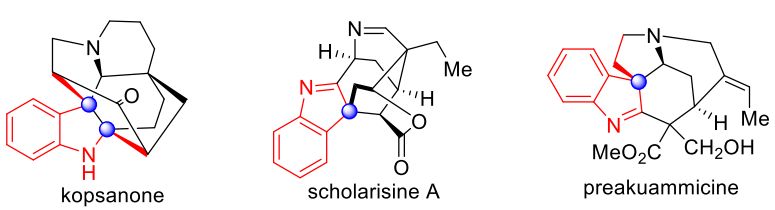
含有多个连续手性中心的螺环吲哚啉生物碱

已有策略和适用范围
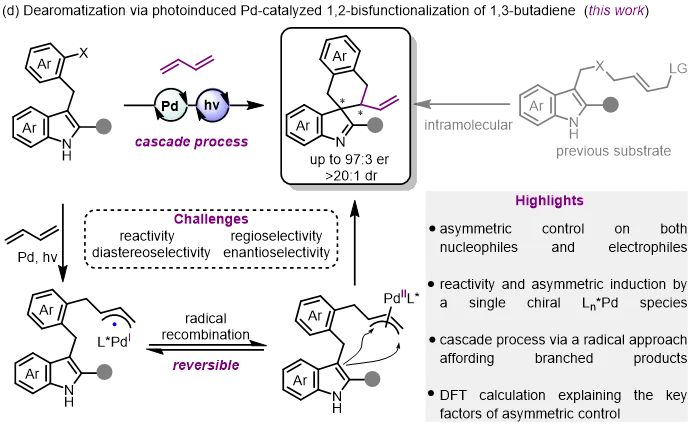
工作设想及亮点
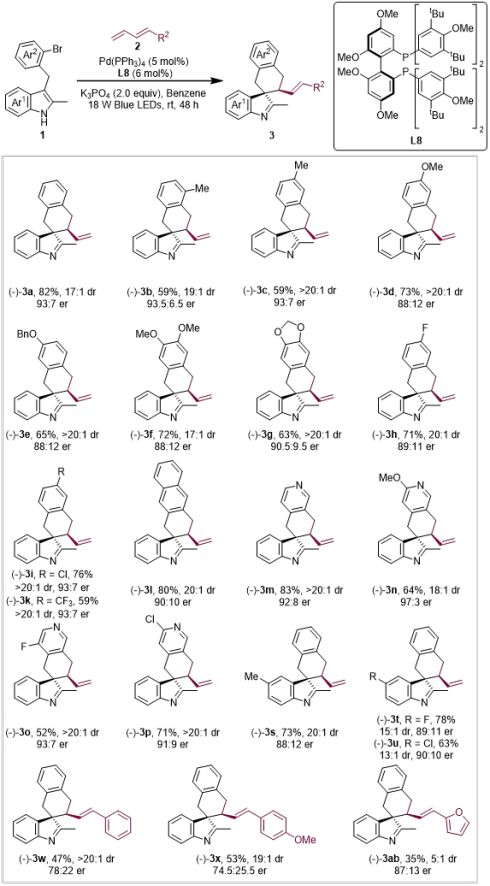
底物范围
阅读原文
